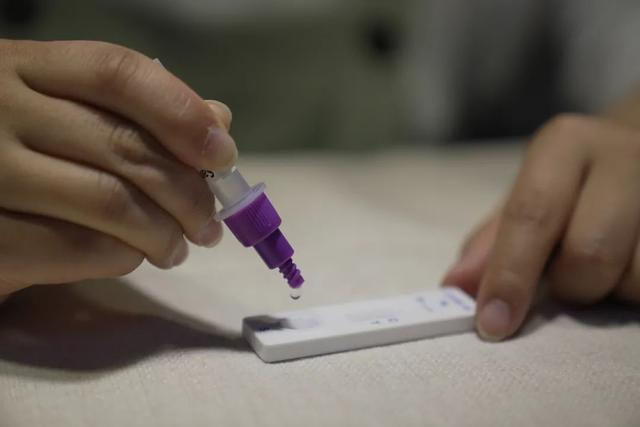
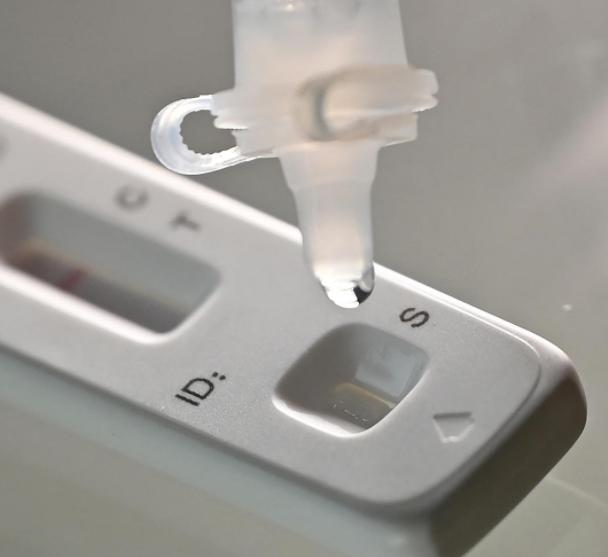
Le 12 marsth 2022, laNMPA (SFDA) a publié un avis approuvant la modification de la demande d'auto-test des produits antigéniques COVID-19 par Nanjing Vazyme BiotechCo., Ltd, Pékin Jinwofu Bioengineering TechnologyCo., Ltd, Technologie pharmaceutique Cie., Ltd de Shenzhen Huada Yinyuan, Guangzhou Wondfo Biotech Co., Ltd etBeijing Savant Biotechnology Co., ltd(Huaketaï).Cinq produits d'autotest d'antigène COVID-19 ont été lancés.
Le 11 mars 2022, le NHC avait annoncé que, afin d'optimiser davantage la stratégie de test du nouveau coronavirus et de répondre aux besoins de prévention et de contrôle du COVID-19, l'équipe complète du mécanisme conjoint de prévention et de contrôle du Conseil d'État a décidé d'ajouter des tests d'antigène aux tests d'acide nucléique et a créé "le protocole d'application pour la détection d'antigène de nouveau coronavirus (essai)"
Le protocole précise la population applicable pour les tests antigéniques :
Premièrement, ceux qui visitent les établissements médicaux primaires et présentent des symptômes tels que des voies respiratoires et de la fièvre dans les 5 jours suivant l'apparition des symptômes ;
Deuxièmement, le personnel d'observation de la quarantaine, y compris l'observation de la quarantaine à domicile, les contacts étroits et les contacts sous-étroits, l'observation de la quarantaine à l'entrée, le personnel de la zone de confinement et de la zone de contrôle ;
Le troisième concerne les résidents de la communauté qui ont besoin d'une auto-détection d'antigènes.
Conseils : la détection d'antigène est un complément important de la détection d'acide nucléique, mais les résultats de l'auto-détection d'antigène ne peuvent pas être utilisés comme base pour le diagnostic d'infection.
Heure de publication : 22 mars 2022